- 定做培养基/定制培养基
- 颗粒培养基
- 标准菌株生化鉴定试剂盒
- 预灌装即用型成品培养基
- 2025年版中国药典
- 促销/特价商品
- 院感/疾控/体外诊断/采样管
- 样品采集与处理(均质)产品
- 按标准检索培养基
- 模拟灌装用培养基
- 干燥粉末培养基
- 培养基添加剂/补充剂
- 生化反应鉴定管
- 染色液等配套产品
- 对照培养基/标准品
- 实验耗材与器具
- 生化试剂/化学试剂
- 菌种鉴定服务
质检中心工器具清洁灭菌效果验证报告
山东拓普生物工程有限公司
Shandong Tuopu Biol-Engineering Co.,Ltd
审批
部门
姓名
签名
日期
起草人
质量检验部
×××
审核人
质量检验部
×××
审核人
品质管理部
×××
审核人
品质管理部
×××
批准人
质量负责人
×××
01 品质管理部(1份)
共计1份
目录
一、总论
二、参考文件
三、验证小组成员与职责
四、验证范围和验证时间计划
五、风险评估
六、验证前准备
七、验证内容
八、偏差处理
九、验证结果评价
十、附件
验证报告
会议与人员签到表
会议地点: 会议时间:
序号
姓名
时间
序号
姓名
时间
备注:
会议记录
部门/组别:品质管理部
时间
地点
会议主持
会议记录人
参会人员
主要议题
会
议
主
要
内
容
一、总论
为保证工器具灭菌效果,避免样品的二次污染,达到实验要求,本次质检中心工器具清洁灭菌效果验证是采用专用湿热灭菌的呼吸袋将所需要灭菌处理的工器具密封,于121℃ 30min高压蒸汽灭菌,待冷却至室温后,采用微生物检测的方法定期来监测其微生物污染水平,收集验证周期内符合要求的储存期限,从而证实被检工器具在有效期内用微生物限度检查法监测后可达到灭菌效果,确认该操作规程可行,使检验工器具二次污染的风险可控,为产品质量提供保障,质检中心工器具储存期限方法验证小组于 年 月 日至 月 日对《质检中心工器具清洁灭菌效果》方法进行了验证,从而确认按《质检中心工器具清洁灭菌操作规程》执行后达到预期要求。
二、参考文件
1 验证管理规程
2 风险管理规程
3 《药品生产质量管理规范》2010年版
4 《药品GMP指南》
三、验证小组成员
组长:
姓名
部门
工作职责
质量检验部
负责起草验证文件
质量检验部
负责审核验证文件,监督验证方案的实施
品质管理部
负责相关文件的审核、归档,确保验证工作照章进行
质量负责人
负责批准验证活动的执行
四、验证范围和验证时间安排
验证范围:质检中心工器具储存期限方法验证相关活动
验证小组于 年 月 日至 月 日按验证方案进行验证
五、风险评估
1 风险识别
C+A级区工器具转移的风险来源:
灭菌后二次受到环境污染;外包装的污染;传递过程污染;操作人员污染;
2 风险分析
目的:风险分析是对已识别的项目的风险进行分析,以确定风险严重程度。
方法:应用失效模式与影响分析,识别潜在的失效模式,对风险发生的概率、严重性和可检测性评分。
3风险评估
3.1风险方法:进行风险评估所用的方法遵循FMEA技术(失效模式与影响分析)包括以
下点。
风险确认:可能影响产品质量、产量、工艺操作或数据完整性的风险。
风险判断:包括评估先前确认风险的后果,其基础建立在严重程度、可能性及可检测性上。
严重程度(S):测定风险潜在的后果,主要针对可能危害产品质量及数据完整性的影响。严重程度分为四个等级
严重性(S)
风险系数
风险可能导致的结果
关键
4
直接影响产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性。此风险可导致产品不能使用;直接影响GMP原则,危害产品生产活动。
高
3
直接影响产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性。此风险可导致产品召回或退回;不符合GMP原则,可能引起检查或审计中产生偏差
中
2
尽管不存在对产品或数据的相关影响,但仍间接影响产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性;此风险可能造成资源的浪费。
低
1
尽管此类风险不对产品或数据产生最终影响,但对产品质量要素或工艺与质量数据的可靠性、完整性或可跟踪性仍产生较小影响
可能性程度(P):测定风险产生的可能性。根据积累的经验、工艺、操作复杂性知识
小组提供的其他目标数据,可获得可能性的数值。
可能性(P)
风险系数
风险可能导致的结果
极高
4
极易发生
高
3
偶尔发生
中
2
很少发生
低
1
发生可能性极低
可检测性(D):在潜在风险造成危害前,检测发现的可能性。
可测性(D)
风险系数
风险可能导致的结果
极低
4
不存在能够检测到错误的机制
低
3
通过周期性控制可检测到错误
中
2
通过应用于每批的常规手动控制或分析可检测到错误
高
1
自动控制装置到位,检测错误(例:警报)或错误明显(例:错误导致不能继续进入下一阶段工艺)
3.2 风险级别评判标准
3.2.1风险优先系数(RPN)计算公式
RPN=SPD=严重性(S)×可能性(P)×可测性(D)
3.2.2风险评价标准
风险优先
系数RPN
风险水平
描述
RPN>16
严重程度=4
高风险水平
此为不可接受风险。必须尽快采用控制措施,通过提高可检测性及降低风险产生的可能性来降低最终风险水平。验证应先集中于确认已采用控制措施且持续执行。
8≤RPN≤16
中等风险水平
此风险要求采用控制措施,通过提高可检测性及(或)降低风险产生的可能性来降低最终风险水平。所采用的措施可以是规程或技术措施,但均应经过验证。
RPN≤7
低风险水平
此风险水平为可接受,无需采用额外的控制措施。
序号
风险项目
失效模式
严重性S
可能性P
可检测性D
RPN
风险等级
风险控制措施
1
转移袋污染
污染A级区环境,威胁到药品质量
3
1
2
6
低
转移袋随工器具同时灭菌
2
传递过程污染
传递过程被C级空气污染污染B级区环境,威胁到药品质量
3
2
2
12
中
扎口密封,穿越C级区后,置A级层流罩净化后使用。
3
培养基的制备
培养基灭菌不彻底
3
2
1
6
低
加强操作工的相关SOP培训,每班次灭菌在纯蒸汽灭菌柜中放置灭菌指示剂或指示条。
4
培养皿的制备
使用前包装完整性的检查遗漏或不彻底
3
3
1
9
中
对员工进行再培训,严格按照规范进行操作。
5
培养皿的浇制
无菌操作失败
3
2
1
6
低
对员工进行再培训,严格按照规范进行操作,每批浇制时对操作工进行表面接触碟的监测。
6
平皿的包装
使用了已污染或破损的包装袋
4
3
2
24
高
浇制好的培养皿用已灭菌的双层包装袋包裹,避免在运输和培养中的污染风险。
7
平皿的检查
检查过程中带入污染
4
2
1
8
中
培养好的空白培养碟,在使用前100%的进行无菌检查,同时对染菌碟进行记录和调查,每批浇制好的碟子都会根据浇制日期,来进行空白碟子的批号管理。
8
检验方法
对检验方法不熟练
3
3
1
9
中
按照表面微生物检验方法及操作规程进行取样操作。
9
收到操作人员污染
整理、放置、转移时被人员污染污染A级区环境,威胁到药品质量
3
3
1
9
中
培训操作人员,严格按卫生操作规程执行,工器具清洁后用呼吸袋包装灭菌、转移。在单向流A级层流罩保护下打开呼吸袋,进行检验。
10
空气质量、单向流、风量、风速、温湿度
所供应的空气质量不当
4
3
2
24
高
确认HEPA过滤器的安装,且维护方案到位,确认关键仪表的校准,按照工艺需求监测空调系统(颗粒等级、微生物控制、HEPA过滤器完整性测试、压差,温湿度等)
六、验证前准备
1 文件确认
序号
文件名称
文件编码
存放地点
1
《纯蒸汽灭菌柜操作规程》
3
《微生物检验管理规程》
4
《非无菌检查微生物限度检查法操作规程》
5
《验证管理规程》
6
《净化工作台操作规程》
7
《质检中心洁净区管理规程》
8
《快速封口机操作规程》
确认人/日期: 复核人/日期:
2 人员培训
序号
培训文件名称
编号
被培训人
培训情况
培训日期
合格□不合格□
合格□不合格□
合格□不合格□
合格□不合格□
合格□不合格□
3 设备、仪器、仪表确认:
序号
检验设备、仪器、仪表
编号
校验有效期
1
生化培养箱
2
生化培养箱
3
纯蒸汽灭菌柜
4
净化工作台
5
压力表
检查人/日期
复核人/日期
4 物料清单:
序号
物料名称
批号/编号
供应商
配制批号
有效期至
1
R2A培养基
2
对照培养基
3
枯草芽孢杆菌
4
铜绿假单胞菌
5
湿热脂肪芽孢杆菌生物指示剂
6
呼吸袋
检查人
日 期
七、验证内容
1 原理
本验证是在工器具灭菌后放置数天,按《纯蒸汽灭菌柜操作规程》进行清洁灭菌后逐日对工器具进行微生物检测,若结果在规定验证标准之内,则可认为工器具在储存期间无菌,不会对检验结果造成影响。
2 验证要求
质检中心工器具清洁灭菌效果与当日检验检品同时进行(连续三批),3次结果必须符合规定,确保检验数据重现性。
2.1 样品的前处理
随机将已清洗好的2个培养皿、2支移液管、2个过滤器、2包滤膜(直经0.45um)、2包封口膜、2个离心管、2个湿热脂肪芽孢杆菌生物指示剂,放入呼吸袋内用封口机密封,同法制得10个相同的灭菌袋放入纯蒸汽灭菌柜中,于121℃30min进行灭菌处理,待冷却至室温后,取出并集中放置于已灭菌工器具暂存柜中,分别在24h、48h……240h,监测其微生物污染水平。
2.2取样部位
名 称
取样部位
取样方法
培养皿
内外表面
擦拭法
移液管
封口膜
离心管
滤膜
2.3 验证可接受标准
目检:表面清洁无残留物、污物或残留物的气味,淋洗水应无色、无味。
微生物限度:棉签取样菌落数<1cfu/棉签(25cm2)。
2.4 取样方法 棉签擦拭法
2.4.1棉签使用前用注射用水预先清洗,以免取样时掉落纤维,使用前应灭菌。
2.4.2 取样前用生无菌理盐水湿润棉签,并挤压棉签除去多余灭菌生理盐水。
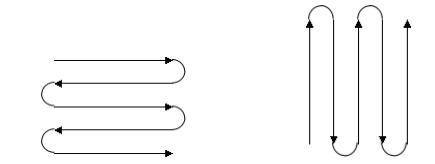
2.4.3将棉签按在取样表面上,用力使其稍弯曲,平稳而缓慢的擦拭取样部位,向前移动的同时将其从一边移到另一边。擦拭过程应覆盖整个表面,翻转棉签,使棉签的另一面也得到擦拭,但与前次擦拭移动方向垂直,见下图。
2.4.5 每个棉签取样面积为25cm2,擦拭结束将棉签放入取样试管,塞紧试管塞。
2.5 样品处理
2.5.1培养皿、离心管、封口膜、过滤器、滤膜:取无菌棉签分别对被测物内外表面进行擦拭取样,擦拭时均匀且充分接触被测物体内外表面,取样结束后将棉签头剪下,加入20ml无菌生理盐水的试管中,充分振荡并按《微生物限度检查法》(薄膜过滤法)进行处理,将滤膜菌面朝上贴于R2A培养基中30~35℃培养5天,观察并记录结果。
2.5.2 移液管:取无菌棉签对移液管外表面进行擦拭取样,擦拭时均匀且充分接触被测物体内外表面,取样结束后将棉签头剪下,加入20ml无菌生理盐水的试管中,充分振荡,再将移液管满量程吸取混合液反复吹洗3次,确保擦拭取样后样液与吹洗样液混合均匀,按《微生物限度检查法》(薄膜过滤法)进行处理,将滤膜菌面朝上贴于R2A培养基中30~35℃培养5天,观察并记录结果。
2.6检验方法
2.6.1外观:目测表面清洁无残留物、污物或残留物的气味;最终淋洗水无色、无味,微生物限度标准<1cfu/100ml。
2.6.2微生物限度测定:按《微生物限度检查法操作规程》(薄膜过滤法)检验。
2.7检验结果
2.7.1 辅助检验记录
2.7.1.1 微生物限度培养基适用性检查记录
培养基名称
工作菌株编号
批号
菌液稀释级
对照培养基批号
传代代次
培养箱型号
培养箱编号
培养温度
培养时间
计数步骤:
1.菌液稀释:取新鲜菌液1接种环至10ml无菌生理盐水中,混匀,逐级等梯度稀释
2.计数结果:取1ml菌液或稀释剂加入已灭菌培养皿内,分别倾注被检培养基与对照培养基,培养并计数。
标准规定:被检固体培养基上的菌落数与对照培养基上的菌落数平均值比值应在0.5~2
范围内,且菌落形态大小应与对照培养基上的一致,试验菌应生长良好。
试验菌种名称:铜绿假单胞菌、枯草芽孢杆菌
铜
绿
假
单
胞
菌
菌液稀释级
10-1
10-2
10-3
10-4
R2A
R2A对照培养基
回收率
枯草芽孢杆菌
菌液稀释级
10-1
10-2
10-3
10-4
R2A
R2A对照培养基
回收率
阴性对照
空白对照
备注:“+”表示长菌“-”表示未长菌
结论:
检查人/日期
复核人/日期
2.7.1.2 灭菌设备灭菌效果记录(一)
设备名称
培养箱型号
型号
灭菌前指示剂颜色
设备编号
生物指示剂名称
灭菌参数
生物指示剂厂家
培养条件
生物指示剂批号
标准规定:根据颜色判断灭菌效果,培养后经过灭菌处理的指示剂全部保持紫色,为灭菌合格。由紫色变成黄色的为灭菌不合格。同时对照管应由紫色变为黄色。
序号
指示剂放置位置
1天
2天
3天
4天
5天
6天
7天
备注
1
2
3
4
5
注: 阴性结果(一)为紫色;阳性结果(+)为黄色
结论:
检验人/日期:
复核人/日期:
灭菌设备灭菌效果记录(二)
设备名称
培养箱型号
型号
灭菌前指示剂颜色
设备编号
生物指示剂名称
灭菌参数
生物指示剂厂家
培养条件
生物指示剂批号
标准规定:根据颜色判断灭菌效果,培养后经过灭菌处理的指示剂全部保持紫色,为灭菌合格。由紫色变成黄色的为灭菌不合格。同时对照管应由紫色变为黄色。
序号
指示剂放置位置
1天
2天
3天
4天
5天
6天
7天
备注
1
2
3
4
5
注: 阴性结果(一)为紫色;阳性结果(+)为黄色
结论:
检验人/日期:
复核人/日期:
灭菌设备灭菌效果记录(三)
备名称
培养箱型号
型号
灭菌前指示剂颜色
设备编号
生物指示剂名称
灭菌参数
生物指示剂厂家
培养条件
生物指示剂批号
标准规定:根据颜色判断灭菌效果,培养后经过灭菌处理的指示剂全部保持紫色,为灭菌合格。由紫色变成黄色的为灭菌不合格。同时对照管应由紫色变为黄色。
序号
指示剂放置位置
1天
2天
3天
4天
5天
6天
7天
备注
1
2
3
4
5
注: 阴性结果(一)为紫色;阳性结果(+)为黄色
结论:
检验人/日期:
复核人/日期:
2.7.2 工器具清洁灭菌效果记录
2.7.2.1 工器具清洁灭菌效果验证外观目检记录(一)
产品名称
规 格
产品批号
清洁日期
取样部位
标准要求
检测结果
培养皿
表面清洁无残留物、污物或残留物的气味,终洗水无色、无味
离心管
封口膜
过滤器
滤膜
结论
检测人/日期
复核人/日期
工器具清洁灭菌效果验证外观目检记录(二)
产品名称
规 格
产品批号
清洁日期
取样部位
标准要求
检测结果
培养皿
表面清洁无残留物、污物或残留物的气味,终洗水无色、无味
离心管
封口膜
过滤器
滤膜
结论
检测人/日期
复核人/日期
工器具清洁灭菌效果验证外观目检记录(三)
产品名称
规 格
产品批号
清洁日期
取样部位
标准要求
检测结果
培养皿
表面清洁无残留物、污物或残留物的气味,终洗水无色、无味
离心管
封口膜
过滤器
滤膜
结论
检测人/日期
复核人/日期
2.7.2.2 工器具清洁淋洗水微生物监测记录(一)
培养基名称
清洗日期
培养基配制批号
集菌仪型号
培养箱型号
培养箱编号
培养温度
培养时间
样品名称
平皿1
平皿2
阴性对照
培养皿淋洗水
离心管淋洗水
过滤器淋洗水
检验人/日期
复核人/日期
工器具清洁淋洗水微生物监测记录(二)
培养基名称
清洗日期
培养基配制批号
集菌仪型号
培养箱型号
培养箱编号
培养温度
培养时间
样品名称
平皿1
平皿2
阴性对照
培养皿淋洗水
离心管淋洗水
过滤器淋洗水
检验人/日期
复核人/日期
工器具清洁淋洗水微生物监测记录(三)
培养基名称
清洗日期
培养基配制批号
集菌仪型号
培养箱型号
培养箱编号
培养温度
培养时间
样品名称
平皿1
平皿2
阴性对照
培养皿淋洗水
离心管淋洗水
过滤器淋洗水
检验人/日期
复核人/日期
2.7.2.3 工器具清洁灭菌效果验证微生物监测记录(一)
产品名称
规 格
产品批号
培养温度
培养箱型号
培养基名称
培养时间
培养基批号
灭菌日期
集菌器型号
保存时限
培养结果
培养皿
离心管
封口膜
过滤器
滤膜
1天
2天
3天
4天
5天
6天
7天
结果
检测人/日期
复核人/日期
工器具清洁灭菌效果验证微生物监测记录(二)
产品名称
规 格
产品批号
培养温度
培养箱型号
培养基名称
培养时间
培养基批号
灭菌日期
集菌器型号
保存时限
培养结果
培养皿
离心管
封口膜
过滤器
滤膜
1天
2天
3天
4天
5天
6天
7天
结果
检测人/日期
复核人/日期
工器具清洁灭菌效果验证微生物监测记录(三)
产品名称
规 格
产品批号
培养温度
培养箱型号
培养基名称
培养时间
培养基批号
灭菌日期
集菌器型号
保存时限
培养结果
培养皿
离心管
封口膜
过滤器
滤膜
1天
2天
3天
4天
5天
6天
7天
结果
检测人/日期
复核人/日期
八、偏差处理
1、验证过程中未预计的问题、偏差、漏项,均应作为原始记录在记录中详细说明。
2、如有偏差或因故无法进行的试验,应进行分析,并由合理的解释说明。
3、当出现偏差时,由品质管理部经分析、确认偏差,执行偏差,执行偏差处理。
九、验证结果及评价
对验证结果进行综合评定的内容包括但不限于以下方面:验证试验结果是否符合标准要求;验证过程是否有偏差及对偏差的说明是否合理;验证试验是否有遗漏;是否需要进一步补充试验;验证记录是否完整。
十、附件
验证报告
验证报告
验证报告编号:E2011-00
验证名称
质检中心工器具清洁灭菌效果验证报告
验证方案名称
质检中心工器具清洁灭菌效
果验证方案
方案编号
F2011-00
验证起止日期
结论:按《质检中心工器具清洁灭菌操作规程》对工器具进行清洁、灭菌后,进行了擦拭取样,经检验,在7天储存期限内其微生物污染水平符合验证要求。
评价与建议:
评价:按《质检中心工器具清洁灭菌操作规程》对工器具进行清洁、灭菌后,进行了擦拭取样,经检验,在7天储存期限内其微生物污染水平符合验证要求,证明《质检中心工器具清洁灭菌操作规程》可行。
建议:若清洗灭菌方式不发生变更,建议再验证周期为2年,若发生变更应重新验证。
验证小组成员会签
批准
签名: 日期:
备注:
验证证书
★★★★★★★★★★★★★★★★★★
验证项目名称:质检中心工器具清洁灭菌效果验证报告
验证方案编号:F2011-00
验证报告编号:E2011-00
已按验证方案完成该项目的验证工作,各项验证结果符合标准要求,经验证委员会审核,批准投入使用。
报告批准日期:
有 效 期:
签发人:
日期:
备注
分发部门:
质检中心工器具清洁灭菌效果,直接影响终产品结果的准确性,因此在进行验证前先对其进行风险分析,在风险分析中确定可能造成本次验证失败或不准确的风险点。本次验证过程中分别由验证小组人员对验证的各项风险项目进行评估,最终的风险评估结果取各个评估人员的平均分,风险控制措施由全体小组成员讨论后确定,本次验证的最终评估结果见下表: